医薬品を取り扱う業者であれば、同時に医療機器を取り扱う機会もありますよね。
昨今注目されている医療機器市場ですが、これまで医療機器は薬事法によって医薬品と同様の規制を受けてきました。
しかし、近年薬事法が改正されて、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(略称:医薬品医療機器等法)」となりました。この改正薬事法によると、医療機器についてはこれまでと異なり、医薬品とは違った取り扱いを受けることとなります。
この改正薬事法による新たな医療機器の取り扱い方法は、これから医療機器を取り扱う業者であれば必須の知識となることは確実です。
そこで今回は、改正された薬事法である医薬品医療機器等法によって医療機器の取り扱いがどのように変わるのかについて解説します。
施行日
まず、改正薬事法の施行日等について確認しておきましょう。
薬事法が改正されて新たに成立した医薬品医療機器等法は、平成25年11月20日に臨時国会にて成立し、平成25年11月27日に公布されました。そして、平成26年11月25日に施行されています。
改正薬事法の名称と略称
次に、改正薬事法の正式名称と略称を確認しておきましょう。
改正薬事法は、正式には「医薬品、医療機器等の品質、有効性及び安全性の確保に関する法律」といいます。これを略して「医薬品医療機器等法」というのが一般的な略称となっています。
よって、今後「医薬品医療機器等法」という法律を見たときは、それは改正された薬事法であるという認識を持たれると良いでしょう。
概要
では、この新たに成立した医薬品医療機器等法の概要を見てみましょう。
①そもそも旧薬事法は昭和18年に成立した法律が、昭和35年に薬剤師法と分離されて現行の薬事法の形になり、現在まで存続してきた古い法律です。
医療機器の規制についても医療用具として、この昭和35年時に医薬品と同様の規制を受けることとされたのです。
しかし、その後の時代の変化の中で科学や医学が発展し、医療機器の形は大きく変わってきました。
薬事法制定時には注射器やカテーテル、体温計などの単なる消耗品が多かった医療用具ですが、近年ではCTスキャン器やMRI撮影機などの医療機械が登場しました。
これらの機械は消耗品ではなく長期にわたって使用されるもので、修理等のメンテナンスも必要となります。
さらに電子医療機器も登場し、パソコンソフトと同様定期的なバージョンアップが必要となったり、プログラムそのものに価値が認められるケースも登場しました。
②そこでこの現状に即して薬事法を改正し、医薬品医療機器等法では医療機器については医薬品とは異なる合理的な取り扱いをして、新たにプログラムそのものも規制対象とすることとしました。
③さらに近年ips細胞などの研究が進んで再生医療が注目されていますが、この医薬品医療機器等法においては、新たに「再生医療等製品」というカテゴリーが設けられ、これについても新たに規制されることとなったのです。
④体外診断用医薬品については、「医薬品」とは言いつつも、医薬品ではなく医療機器と同様の取り扱いをすることとされました。
体外診断用医薬品は、海外では体外診断用医薬品が「メディカルデバイス」として医療機器と同様の扱いを受けているため、国際標準に適合するため従来から医療機器と同様の取り扱いを受けていたものです。
そこで、このたびの法改正においても、体外診断用医薬品の製造販売承認については医療機器と同様の扱いを受けることとしました。ただ、品質管理については医薬品と同様のレベルのものが必要とされるので「医薬品」というカテゴリーそのものには変更は加えませんでした。
薬事法から医薬品医療機器等法に変更されたときのポイント
では、薬事法から医薬品医療機器等法に改正されたときのポイントはどのようなものでしょうか。医療機器と再生医療品製品に分けて見てみましょう。
医療機器について
① まず、医療機器の製造については、国内の製造業は許可制、外国の製造業は認定制が採用されていました。しかし医薬品医療機器法では登録制に変更されています。さらにこれまでは許可不要であった「設計」についても新たに登録が必要とされました。
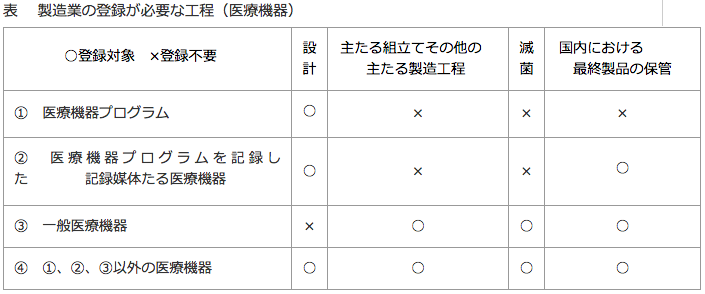
引用先:東京都健康安全研究センター
② 医療機器にはそのリスクによって高度管理医療機器、管理医療機器、一般医療機器の3分類がなされています。
このうち高度管理医療機器の製造販売については、旧薬事法では必ず厚生労働大臣の認証を受けなければならないとされていました。
しかし医薬品医療機器法においては、厚生労働大臣が基準を定めて指定した高度管理医療機器については、厚生労働大臣の登録を受けた第三者認証機関による認証を受けることとなりました。
これは、医療機器の承認手続きを合理化し、医療機器類の開発発展を促進する目的によるものです。
具体的には、歯科インプラントやコンタクトレンズなどの品目が検討対象となっています。

引用先:医薬品医療機器法とは
③ さらに、医療機器等を販売する際、2つの条件を満たした一定の場合には、添付文書の製品への添付を省略することができることとなりました。その2つの条件とは
ⅰ添付文書への記載事項をPMDAのHP上に掲載すること等
ⅱ医療機器等の販売先の医療機関等による承諾を得ていること
です。
④ 添付文書の位置づけについても規定されました。具体的には、医薬品等の製造販売業者は最新の知見に基づき添付文書を作成して厚生労働大臣に届け出ることとして、迅速な情報提供を行うために、その届け出た添付文書をすぐウェブサイトに掲載する必要があります。
⑤ 賃貸業については規制が強められました。旧薬事法では、「業として」医療機器等の賃貸を行う場合は、許可や届出が必要でしたが、医薬品医療機器等法では「業として」ではなく反復継続的に「対価なしに」貸与する場合であっても許可又は届出の規制を要することとしました。
⑥ 重要なのが単体プログラムを医療機器として取り扱う点です。
薬事法では規制対象外となっていた「プログラム」そのものについても規制されることとなったのです。まず、医療機器の定義に「プログラム」や「プログラムを記録した記録媒体」が追加されました。
このプログラム規制においては、疾病の予防や治療、診断用のプログラムやその媒体が対象となります。
製造販売においては、他の医療機器同様に許可を得る必要があります。
製造業として登録対象となる場合もあります。
プログラムの法定表示や添付文書についても他の医療機器と同様規定が設けられています。
医療機器プログラムを電気通信回線を通じて提供する場合は販売業として取り扱われますので、許可や届出が必要になります。プログラムの記録媒体の販売についても同様です。
再生医療等製品について
次に医薬品医療機器等法により規制されることとなった再生医療品製品について見てみましょう。
① 再生医療等製品とは、人間又は動物の医療に使われる目的で、人間又は動物の細胞に培養等の加工を施したもののことです。
ここで再生医療等製品の目的とされる医療は、身体の構造や機能の再建、修復や形成、病気治療や予防、遺伝子治療を目的として人の細胞に導入するものなどです。
再生医療等製品の具体例としては、受精卵から作成された細胞であるES細胞(胚性幹細胞)や、体細胞に特定の遺伝子を入れて作成された細胞であるips細胞、生物がもともと持っている体性幹細胞や体性幹細胞以外の体細胞が考えられています。
② 規制内容としては、まず、均質でない再生医療等製品については、その有効性が推定されて安全性が確認されれば、条件・期限付きではありますが、特別に早期に承認できる仕組みが導入されました。この場合の有効性安全性については、承認後に有効性・安全性を改めて検証することとされています。
③ また、販売先医師等が適切な説明に努めたり、使用についての調査報告、記録保存などについて定めがもうけられたりしています。
④ 健康被害があれば、副作用や感染被害の救済制度対象となりますし、製造管理や品質管理の基準ももうけられて品質・安全性等が確保されます。
⑤ 日本では原則として業として人から採血をすることは禁じられていますが、再生医療等製品の製造業者や医療機関については、人の体から採血した血液を用いて製品を製造することが明確に認められています。
⑥ 販売については、再生医療等製品の販売業の許可を都道府県知事から受けなければならないこととなりました。
⑦ また、再生医療等製品の製造業者は、製造所ごとに、厚生労働大臣の承認を受けた再生医療等製品製造管理者という技術者を置かなければならないこととされています。
⑧ 再生医療等製品の販売営業所の設備についても、衛生的であり、取扱品目を安全に保管するために必要な設備があることなどの基準が設けられています。
まとめ
以上、薬事法が改正されて制定、交付、施行された「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(医薬品医療機器等法)について解説してきましたが、いかがでしたでしょうか。
医療機器の取り扱いについてはその発展促進のために取り扱いを合理化するとともに現状に即した規制も行うこととし、新たにプログラムそのものや再生医療品等製品の規制も行われることとなりました。
これから注目される分野である医療機器や再生医療品の取り扱いを安全に行うためにも、ぜひともこの新しい医薬品医療機器等法のポイントをしっかり押さえておきましょう。












コメント